Termodynamika je dôležitým odvetvím fyziky. Môžeme s istotou povedať, že jeho úspechy viedli k vzniku technologickej éry a do značnej miery určovali priebeh ľudskej histórie za posledných 300 rokov. Článok pojednáva o prvom, druhom a treťom zákone termodynamiky a ich aplikácii v praxi.
Čo je termodynamika?
Skôr ako sformulujeme zákony termodynamiky, poďme zistiť, čo robí táto časť fyziky.
Slovo „termodynamika“je gréckeho pôvodu a znamená „pohyb spôsobený teplom“. To znamená, že toto odvetvie fyziky sa zaoberá štúdiom akýchkoľvek procesov, v dôsledku ktorých sa tepelná energia premieňa na mechanický pohyb a naopak.
Základné zákony termodynamiky boli sformulované v polovici 19. storočia. Veda o "pohybe a teple" zvažuje správanie celého systému ako celku, študuje zmenu jeho makroskopických parametrov - teploty, tlaku a objemu a nevenuje pozornosť jeho mikroskopickej štruktúre. Navyše, prvý z nich hrá zásadnú úlohu pri formulovaní zákonovtermodynamika vo fyzike. Je zaujímavé poznamenať, že sú odvodené výlučne z experimentálnych pozorovaní.
Koncept termodynamického systému

To znamená akúkoľvek skupinu atómov, molekúl alebo iných prvkov, ktoré sa považujú za jeden celok. Všetky tri zákony sú formulované pre takzvaný termodynamický systém. Príkladmi sú: zemská atmosféra, akýkoľvek živý organizmus, zmes plynov v spaľovacom motore atď.
Všetky systémy v termodynamike patria do jedného z troch typov:
- Otvorené. Vymieňajú si teplo aj hmotu s prostredím. Napríklad, ak sa jedlo varí v hrnci na otvorenom ohni, potom je to názorný príklad otvoreného systému, pretože hrniec prijíma energiu z vonkajšieho prostredia (oheň), pričom sám vyžaruje energiu vo forme tepla, a tiež sa z neho vyparuje voda (metabolizmus).
- Zatvorené. V takýchto systémoch nedochádza k výmene hmoty s prostredím, hoci k výmene energie dochádza. Vráťme sa k predchádzajúcemu prípadu: ak kanvicu zakryjete pokrievkou, môžete získať uzavretý systém.
- Izolovaný. Ide o druh termodynamických systémov, ktoré si nevymieňajú hmotu ani energiu s okolitým priestorom. Príkladom môže byť termoska s horúcim čajom.
Termodynamická teplota

Tento pojem znamená kinetickú energiu častíc, ktoré tvoria okolité telesá, ktorá odráža rýchlosťnáhodný pohyb častíc. Čím je väčšia, tým vyššia je teplota. Znižovaním kinetickej energie systému ho teda chladíme.
Tento pojem znamená kinetickú energiu častíc, ktoré tvoria okolité telesá, ktorá odráža rýchlosť chaotického pohybu častíc. Čím je väčšia, tým vyššia je teplota. Znižovaním kinetickej energie systému ho teda chladíme.
Termodynamická teplota je vyjadrená v SI (International System of Units) v Kelvinoch (na počesť britského vedca Williama Kelvina, ktorý ako prvý navrhol túto stupnicu). Pochopenie prvého, druhého a tretieho zákona termodynamiky je nemožné bez definície teploty.
Rozdelenie jedného stupňa na Kelvinovej stupnici tiež zodpovedá jednému stupňu Celzia. Prepočet medzi týmito jednotkami sa vykonáva podľa vzorca: TK =TC + 273, 15, kde TK a TC - teploty v kelvinoch a stupňoch Celzia.
Zvláštnosťou Kelvinovej stupnice je, že nemá záporné hodnoty. Nula v ňom (TC=-273, 15 oC) zodpovedá stavu, keď tepelný pohyb častíc systému úplne chýba, zdá sa, že sú „zamrznuté“.
Zachovanie energie a 1. zákon termodynamiky

V roku 1824 Nicolas Léonard Sadi Carnot, francúzsky inžinier a fyzik, predložil odvážny návrh, ktorý viedol nielen k rozvoju fyziky, ale stal sa aj významným krokom v zlepšovaní technológie. Jehomožno formulovať takto: „Energia nemôže byť vytvorená ani zničená, môže byť iba prenesená z jedného stavu do druhého.“
Fráza Sadiho Carnota v skutočnosti postuluje zákon zachovania energie, ktorý tvoril základ 1. zákona termodynamiky: „Kedykoľvek systém prijíma energiu zvonku, premieňa ju na iné formy, hlavné ktoré sú tepelné a mechanické."
Matematický vzorec pre 1. zákon je napísaný takto:
Q=ΔU + A, tu Q je množstvo tepla preneseného prostredím do systému, ΔU je zmena vnútornej energie tohto systému, A je dokonalá mechanická práca.
Adiabatické procesy
Dobrým príkladom je pohyb vzdušných hmôt pozdĺž horských svahov. Takéto masy sú obrovské (kilometre alebo viac) a vzduch je vynikajúcim tepelným izolantom. Uvedené vlastnosti nám umožňujú považovať akékoľvek procesy so vzduchovými hmotami, ktoré sa vyskytujú v krátkom čase, za adiabatické. Keď vzduch stúpa na horský svah, jeho tlak klesá, expanduje, to znamená, že vykonáva mechanickú prácu a v dôsledku toho sa ochladzuje. Naopak, pohyb vzdušnej hmoty nadol je sprevádzaný zvýšením tlaku v nej, stláča sa a vďaka tomu sa veľmi zahrieva.
Aplikáciu zákona termodynamiky, o ktorej sme hovorili v predchádzajúcom podnadpise, možno najjednoduchšie demonštrovať na príklade adiabatického procesu.
Podľa definície nedochádza k výmene energie sprostredia, to znamená vo vyššie uvedenej rovnici Q=0. To vedie k nasledujúcemu výrazu: ΔU=-A. Znamienko mínus tu znamená, že systém vykonáva mechanickú prácu znížením vlastnej vnútornej energie. Je potrebné pripomenúť, že vnútorná energia je priamo závislá od teploty systému.
Smer tepelných procesov
Toto číslo sa zaoberá 2. termodynamickým zákonom. Každý si určite všimol, že ak privediete do kontaktu dva predmety s rôznou teplotou, studený sa vždy zahreje a horúci vychladne. Všimnite si, že opačný proces môže nastať v rámci prvého zákona termodynamiky, ale v praxi sa nikdy neuplatňuje.
Dôvodom nezvratnosti tohto procesu (a všetkých známych procesov vo Vesmíre) je prechod systému do pravdepodobnejšieho stavu. V uvažovanom príklade s kontaktom dvoch telies rôznych teplôt bude najpravdepodobnejší stav, v ktorom budú mať všetky častice systému rovnakú kinetickú energiu.
Druhý zákon termodynamiky možno formulovať takto: "Teplo sa nikdy nemôže samovoľne preniesť zo studeného telesa na horúce." Ak zavedieme pojem entropia ako mieru neusporiadanosti, potom ju možno znázorniť takto: „Akýkoľvek termodynamický proces prebieha so zvýšením entropie“.
Tepelný motor

Tento pojem sa chápe ako systém, ktorý vďaka dodávke vonkajšej energie do neho môže vykonávať mechanickú prácu. najprvtepelné motory boli parné stroje a boli vynájdené na konci 17. storočia.
Pri určovaní ich účinnosti zohráva rozhodujúcu úlohu druhý termodynamický zákon. Sadi Carnot tiež zistil, že maximálna účinnosť tohto zariadenia je: Účinnosť=(T2 - T1)/T2, tu T2 a T1 sú teploty ohrievača a chladničky. Mechanickú prácu je možné vykonávať iba vtedy, keď dochádza k toku tepla z horúceho telesa do studeného a tento tok nemožno na 100 % premeniť na užitočnú energiu.
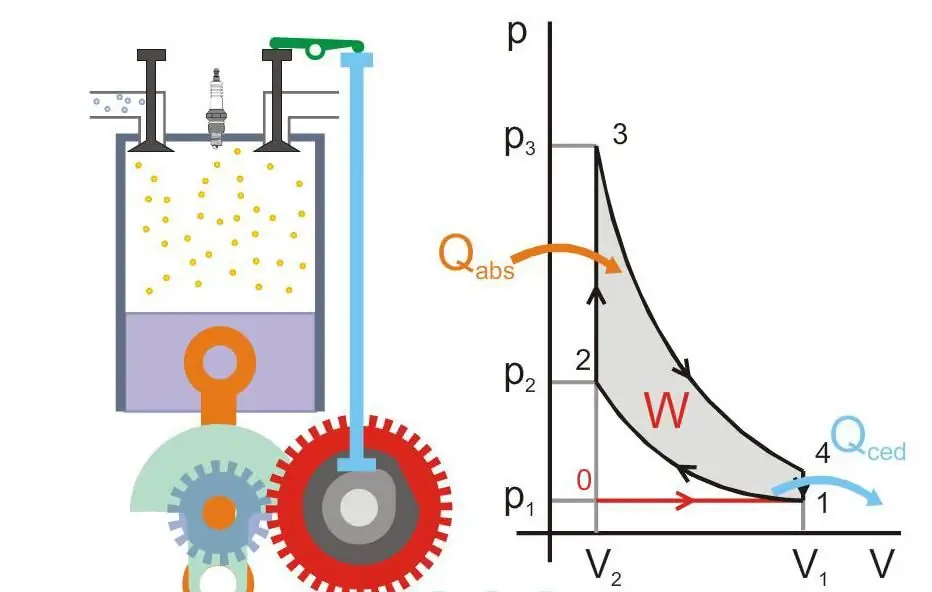
Na obrázku nižšie je znázornený princíp činnosti tepelného motora (Qabs - teplo prenášané do stroja, Qced - tepelné straty, W - užitočná práca, P a V - tlak a objem plynu v pieste).
Absolútna nula a Nernstov postulát
Na záver prejdime k úvahe o treťom termodynamickom zákone. Nazýva sa aj Nernstov postulát (meno nemeckého fyzika, ktorý ho prvýkrát sformuloval na začiatku 20. storočia). Zákon hovorí: "Absolútnu nulu nemožno dosiahnuť konečným počtom procesov." To znamená, že je nemožné akýmkoľvek spôsobom úplne „zmraziť“molekuly a atómy látky. Dôvodom je neustála výmena tepla s okolím.

Jedným užitočným záverom z tretieho zákona termodynamiky je, že entropia klesá, keď sa človek pohybuje smerom k absolútnej nule. To znamená, že systém má tendenciu organizovať sa sám. Táto skutočnosť môžepoužiť napríklad na prenos paramagnetov do feromagnetického stavu po ochladení.
Je zaujímavé poznamenať, že najnižšia teplota, ktorá bola doteraz dosiahnutá, je 5·10−10 K (2003, laboratórium MIT, USA).






