Pri štúdiu správania sa plynov vo fyzike sa veľká pozornosť venuje izoprocesom, teda takým prechodom medzi stavmi systému, pri ktorých je zachovaný jeden termodynamický parameter. Medzi stavmi však dochádza k prechodu plynu, ktorý nie je izoprocesom, ale hrá dôležitú úlohu v prírode a technológii. Toto je adiabatický proces. V tomto článku sa ním budeme zaoberať podrobnejšie a zameriame sa na to, čo je adiabatický exponent plynu.
Adiabatický proces
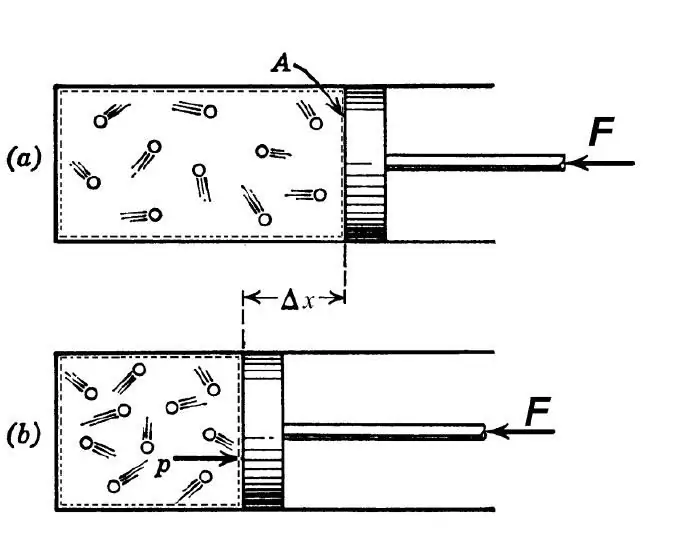
Adiabatický proces je podľa termodynamickej definície chápaný ako taký prechod medzi počiatočným a konečným stavom systému, v dôsledku ktorého nedochádza k výmene tepla medzi vonkajším prostredím a skúmaným systémom. Takýto proces je možný za nasledujúcich dvoch podmienok:
- tepelná vodivosť medzi vonkajším prostredím asystém je z jedného alebo druhého dôvodu slabý;
- rýchlosť procesu je vysoká, takže výmena tepla nestihne nastať.
V strojárstve sa adiabatický prechod používa na zahriatie plynu počas jeho prudkého stlačenia a na jeho ochladenie počas rýchlej expanzie. V prírode sa predmetný termodynamický prechod prejaví, keď vzduchová hmota stúpa alebo klesá zo svahu. Takéto vzostupy a pády vedú k zmene rosného bodu vo vzduchu a zrážok.
Poissonova rovnica pre adiabatický ideálny plyn

Ideálny plyn je systém, v ktorom sa častice pohybujú náhodne vysokou rýchlosťou, vzájomne neinteragujú a sú bezrozmerné. Takýto model je z hľadiska jeho matematického popisu veľmi jednoduchý.
Podľa definície adiabatického procesu môže byť nasledujúci výraz napísaný v súlade s prvým zákonom termodynamiky:
dU=-PdV.
Inými slovami, plyn, expandujúci alebo zmršťujúci, pracuje PdV v dôsledku zodpovedajúcej zmeny jeho vnútornej energie dU.
V prípade ideálneho plynu, ak použijeme stavovú rovnicu (Clapeyronov-Mendelejevov zákon), môžeme dostať nasledujúci výraz:
PVγ=const.
Táto rovnosť sa nazýva Poissonova rovnica. Ľudia, ktorí sú oboznámení s fyzikou plynov, si všimnú, že ak je hodnota γ rovná 1, potom Poissonova rovnica prejde do Boyleovho-Mariottovho zákona (izotermickáproces). Takáto transformácia rovníc je však nemožná, pretože γ pre akýkoľvek typ ideálneho plynu je väčšie ako jedna. Množstvo γ (gama) sa nazýva adiabatický index ideálneho plynu. Pozrime sa bližšie na jeho fyzický význam.
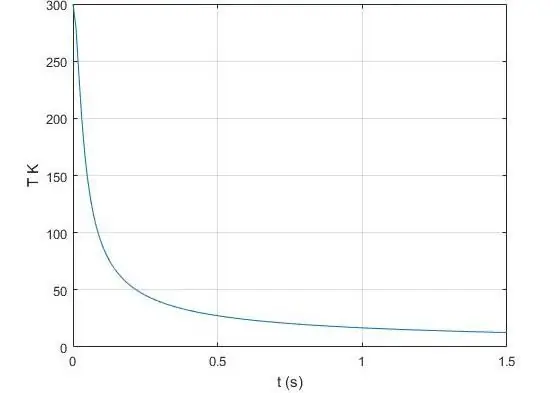
Aký je adiabatický exponent?
Exponent γ, ktorý sa objavuje v Poissonovej rovnici pre ideálny plyn, je pomer tepelnej kapacity pri konštantnom tlaku k rovnakej hodnote, ale už pri konštantnom objeme. Vo fyzike je tepelná kapacita množstvo tepla, ktoré sa musí odovzdať alebo odobrať z daného systému, aby zmenil svoju teplotu o 1 Kelvin. Izobarickú tepelnú kapacitu budeme označovať symbolom CP a izochorickú tepelnú kapacitu symbolom CV. Potom platí rovnosť pre γ:
γ=CP/CV.
Keďže γ je vždy väčšie ako jedna, ukazuje, koľkokrát izobarická tepelná kapacita študovaného plynového systému prevyšuje podobnú izochorickú charakteristiku.
Tepelné kapacity CP a CV
Na určenie adiabatického exponentu je potrebné dobre pochopiť význam veličín CP a CV. Aby sme to dosiahli, vykonáme nasledujúci myšlienkový experiment: predstavte si, že plyn je v uzavretom systéme v nádobe s pevnými stenami. Ak sa nádoba zahrieva, potom sa všetko odovzdané teplo v ideálnom prípade premení na vnútornú energiu plynu. V takejto situácii bude platiť rovnosť:
dU=CVdT.
HodnotaCVdefinuje množstvo tepla, ktoré musí byť odovzdané systému, aby sa izochoricky ohrialo o 1 K.
Teraz predpokladajme, že plyn je v nádobe s pohyblivým piestom. V procese zahrievania takéhoto systému sa piest bude pohybovať, čím sa zabezpečí udržiavanie konštantného tlaku. Keďže entalpia systému sa v tomto prípade bude rovnať súčinu izobarickej tepelnej kapacity a zmeny teploty, prvý zákon termodynamiky bude mať tvar:
CPdT=CVdT + PdV.
Odtiaľto je vidieť, že CP>CV, keďže v prípade izobarickej zmeny stavov je potrebné vynaložiť teplo nielen na zvýšenie teploty systému, a tým aj jeho vnútornej energie, ale aj na prácu, ktorú vykoná plyn počas jeho expanzie.
Hodnota γ pre ideálny monatomický plyn
Najjednoduchší plynový systém je monatomický ideálny plyn. Predpokladajme, že máme 1 mól takého plynu. Pripomeňme, že v procese izobarického ohrevu 1 mol plynu iba o 1 Kelvin funguje rovno R. Tento symbol sa bežne používa na označenie univerzálnej plynovej konštanty. Rovná sa 8, 314 J / (molK). Aplikovaním posledného výrazu v predchádzajúcom odseku pre tento prípad dostaneme nasledujúcu rovnosť:
CP=CV+ R.
Odkiaľ môžete určiť hodnotu izochorickej tepelnej kapacity CV:
γ=CP/CV;
CV=R/(γ-1).
Je známe, že na jedného krtkamonatomický plyn, hodnota izochorickej tepelnej kapacity je:
CV=3/2R.
Z posledných dvoch rovníc vyplýva hodnota adiabatického exponentu:
3/2R=R/(γ-1)=>
γ=5/3 ≈ 1, 67.
Všimnite si, že hodnota γ závisí výlučne od vnútorných vlastností samotného plynu (od polyatomickej povahy jeho molekúl) a nezávisí od množstva látky v systéme.
Závislosť γ od počtu stupňov voľnosti
Rovnica pre izochorickú tepelnú kapacitu monatomického plynu bola napísaná vyššie. Koeficient 3/2, ktorý sa v ňom objavil, súvisí s počtom stupňov voľnosti v jednom atóme. Má schopnosť pohybovať sa iba jedným z troch smerov priestoru, to znamená, že existujú iba translačné stupne voľnosti.
Ak je systém tvorený dvojatómovými molekulami, potom sa k trom translačným stupňom pridajú ďalšie dva rotačné stupne. Preto výraz pre CV bude:
CV=5/2R.
Hodnota γ potom bude:
γ=7/5=1, 4.
Všimnite si, že dvojatómová molekula má v skutočnosti ešte jeden vibračný stupeň voľnosti, ale pri teplotách niekoľko stoviek Kelvinov sa neaktivuje a neprispieva k tepelnej kapacite.
Ak molekuly plynu pozostávajú z viac ako dvoch atómov, budú mať 6 stupňov voľnosti. Adiabatický exponent sa v tomto prípade bude rovnať:
γ=4/3 ≈ 1, 33.
TakžeSo zvyšujúcim sa počtom atómov v molekule plynu teda klesá hodnota γ. Ak vytvoríte adiabatický graf v osiach P-V, všimnete si, že krivka pre monatomický plyn sa bude správať ostrejšie ako pre polyatomický.
Adiabatický exponent pre zmes plynov
Vyššie sme ukázali, že hodnota γ nezávisí od chemického zloženia plynového systému. Závisí to však od počtu atómov, ktoré tvoria jeho molekuly. Predpokladajme, že systém pozostáva z N komponentov. Atómový podiel zložky i v zmesi je ai. Potom na určenie adiabatického exponentu zmesi môžete použiť nasledujúci výraz:
γ=∑i=1N(aiγ i).
Kde γi je hodnota γ pre i-tý komponent.
Tento výraz možno napríklad použiť na určenie γ vzduchu. Keďže sa skladá z 99% dvojatómových molekúl kyslíka a dusíka, jeho adiabatický index by mal byť veľmi blízko hodnote 1,4, čo potvrdzuje aj experimentálne stanovenie tejto hodnoty.






