Znalosť definícií vo fyzike je kľúčovým faktorom pre úspešné riešenie rôznych fyzikálnych problémov. V článku zvážime, čo znamená izobarické, izochorické, izotermické a adiabatické procesy pre ideálny plynový systém.
Ideálny plyn a jeho rovnica
Skôr ako pristúpime k popisu izobarických, izochorických a izotermických procesov, pouvažujme, čo je ideálny plyn. Pod touto definíciou vo fyzike považujú systém pozostávajúci z obrovského množstva bezrozmerných a neinteragujúcich častíc, ktoré sa pohybujú vysokou rýchlosťou vo všetkých smeroch. V skutočnosti hovoríme o plynnom agregovanom stave hmoty, v ktorom vzdialenosti medzi atómami a molekulami ďaleko presahujú ich veľkosti a v ktorom je potenciálna energia interakcie častíc v porovnaní s kinetickou energiou zanedbaná pre svoju malú veľkosť.
Stav ideálneho plynu je súhrn jeho termodynamických parametrov. Hlavnými sú teplota, objem a tlak. Označme ich písmenami T, V a P. V 30-tych rokoch XIX storočiaClapeyron (francúzsky vedec) najprv napísal rovnicu, ktorá kombinuje uvedené termodynamické parametre v rámci jedinej rovnosti. Vyzerá to takto:
PV=nRT,
kde n a R sú množstvo látok a konštanta plynu.
Čo sú izoprocesy v plynoch?
Ako si mnohí všimli, izobarické, izochorické a izotermické procesy používajú vo svojich názvoch rovnakú predponu „iso“. Znamená to zhodnosť jedného termodynamického parametra počas prechodu celého procesu, pričom ostatné parametre sa menia. Napríklad izotermický proces naznačuje, že v dôsledku toho sa absolútna teplota systému udržiava konštantná, zatiaľ čo izochorický proces naznačuje konštantný objem.
Izoprocesy sú vhodné na štúdium, pretože stanovenie jedného z termodynamických parametrov vedie k zjednodušeniu všeobecnej rovnice stavu plynu. Je dôležité poznamenať, že zákony plynu pre všetky tieto izoprocesy boli objavené experimentálne. Ich analýza umožnila Clapeyronovi získať redukovanú univerzálnu rovnicu.
Izobarické, izochorické a izotermické procesy
Prvý zákon bol objavený pre izotermický proces v ideálnom plyne. Teraz sa to nazýva Boyleov-Mariottov zákon. Keďže T sa nemení, stavová rovnica implikuje rovnosť:
PV=konšt.
Inými slovami, akákoľvek zmena tlaku v systéme vedie k nepriamo úmernej zmene jeho objemu, ak je teplota plynu udržiavaná konštantná. Graf funkcie P(V) jehyperbola.
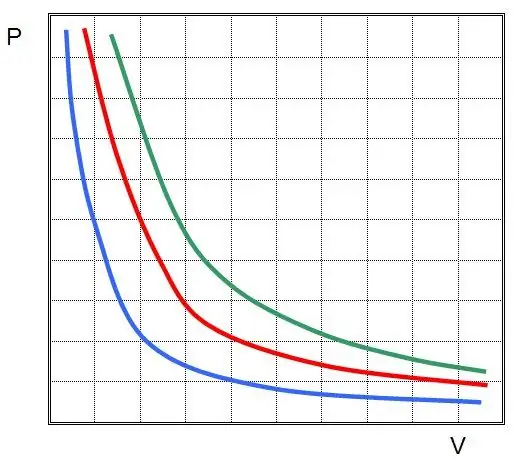
Izobarický proces - ide o zmenu stavu systému, v ktorom tlak zostáva konštantný. Po zafixovaní hodnoty P v Clapeyronovej rovnici dostaneme nasledujúci zákon:
V/T=konšt.
Táto rovnosť nesie meno francúzskeho fyzika Jacquesa Charlesa, ktorý ju dostal na konci 18. storočia. Izobara (grafické znázornenie funkcie V(T)) vyzerá ako priamka. Čím väčší tlak v systéme, tým rýchlejšie táto čiara stúpa.
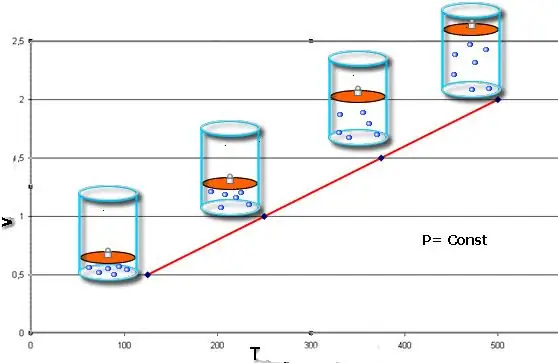
Izobarický proces sa dá ľahko implementovať, ak sa plyn zahrieva pod piestom. Molekuly druhého z nich zvyšujú svoju rýchlosť (kinetickú energiu), vytvárajú vyšší tlak na piest, čo vedie k expanzii plynu a udržiavaniu konštantnej hodnoty P.
Napokon, tretí izoproces je izochorický. Beží s konštantnou hlasitosťou. Zo stavovej rovnice dostaneme zodpovedajúcu rovnosť:
P/T=konšt.
Medzi fyzikmi je známy ako Gay-Lussacov zákon. Priama úmernosť medzi tlakom a absolútnou teplotou naznačuje, že graf izochorického procesu, podobne ako graf izobarického, je priamka s kladným sklonom.
Je dôležité pochopiť, že všetky izoprocesy sa vyskytujú v uzavretých systémoch, to znamená, že hodnota n sa počas ich priebehu zachováva.
Adiabatický proces
Tento proces nepatrí do kategórie „iso“, pretože všetky tri termodynamické parametre sa počas jeho prechodu menia. adiabatickénazývaný prechod medzi dvoma stavmi sústavy, v ktorých si nevymieňa teplo s okolím. Rozšírenie systému sa teda uskutočňuje v dôsledku jeho vnútorných energetických zásob, čo vedie k výraznému poklesu tlaku a absolútnej teploty v ňom.
Adiabatický proces pre ideálny plyn je popísaný Poissonovými rovnicami. Jeden z nich je zobrazený nižšie:
PVγ=const,
kde γ je pomer tepelných kapacít pri konštantnom tlaku a pri konštantnom objeme.
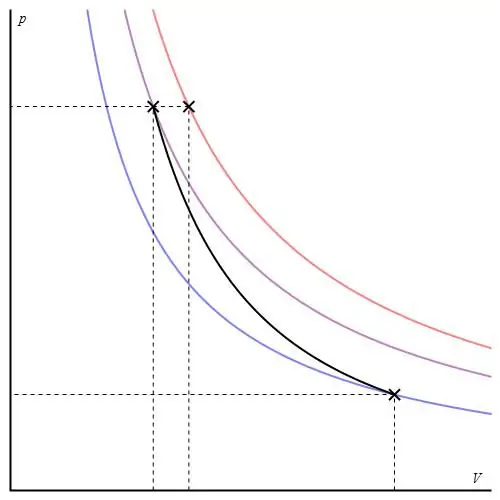
Adiabatický graf sa líši od grafu izochorického procesu a od izobarického grafu, ale je podobný hyperbole (izoterme). Adiabat v osiach P-V sa chová ostrejšie ako izoterma.






