Ideálny plyn, stavová rovnica ideálneho plynu, jeho teplota a tlak, objem… v zozname parametrov a definícií použitých v príslušnej časti fyziky by sa dalo pokračovať ešte dlho. Dnes budeme hovoriť len na túto tému.
Čo sa považuje za molekulárnu fyziku?

Hlavným predmetom, o ktorom sa uvažuje v tejto časti, je ideálny plyn. Stavová rovnica ideálneho plynu bola získaná pri zohľadnení normálnych podmienok prostredia a o tom budeme hovoriť o niečo neskôr. Teraz pristúpme k tomuto „problému“z diaľky.
Povedzme, že máme nejaké množstvo plynu. Jeho stav možno určiť pomocou troch parametrov termodynamického charakteru. Tými sú, samozrejme, tlak, objem a teplota. Rovnica stavu systému v tomto prípade bude vzorcom pre vzťah medzi zodpovedajúcimi parametrami. Vyzerá to takto: F (p, V, T)=0.
Po prvýkrát sa tu pomaly blížime ku vzniku niečoho ako ideáluplynu. Nazýva sa to plyn, v ktorom sú interakcie medzi molekulami zanedbateľné. Vo všeobecnosti to v prírode neexistuje. Každý vysoko riedky plyn je však blízko k nemu. Dusík, kyslík a vzduch, ktoré sú za normálnych podmienok, sa len málo líšia od ideálu. Na napísanie stavovej rovnice pre ideálny plyn môžeme použiť jednotný zákon o plyne. Získame: pV/T=konšt.
Súvisiaci koncept 1: Avogadrov zákon
Môže nám povedať, že ak vezmeme rovnaký počet mólov absolútne akéhokoľvek náhodného plynu a umiestnime ich do rovnakých podmienok, vrátane teploty a tlaku, potom plyny zaberú rovnaký objem. Konkrétne sa experiment uskutočnil za normálnych podmienok. To znamená, že teplota bola 273,15 Kelvina, tlak jedna atmosféra (760 milimetrov ortuti alebo 101325 Pascalov). Pri týchto parametroch zaberal plyn objem rovný 22,4 litra. Preto môžeme povedať, že pre jeden mól akéhokoľvek plynu bude pomer číselných parametrov konštantná hodnota. Preto bolo rozhodnuté označiť tento údaj písmenom R a nazvať ho univerzálna plynová konštanta. Čiže sa rovná 8,31. Jednotkou je J/molK.
Ideálny plyn. Stavová rovnica ideálneho plynu a jej manipulácia
Skúsme prepísať vzorec. Aby sme to dosiahli, zapíšeme ho v tomto tvare: pV=RT. Ďalej vykonáme jednoduchú akciu, vynásobíme obe strany rovnice ľubovoľným počtom mólov. Získame pVu=uRT. Zoberme do úvahy skutočnosť, že súčin molárneho objemu amnožstvo hmoty je jednoducho objem. Koniec koncov, počet mólov sa bude súčasne rovnať podielu hmotnosti a molárnej hmotnosti. Presne takto vyzerá Mendelejevova-Clapeyronova rovnica. Poskytuje jasnú predstavu o tom, aký druh systému tvorí ideálny plyn. Stavová rovnica pre ideálny plyn bude mať tvar: pV=mRT/M.
Odvodiť vzorec pre tlak
Urobme ďalšie manipulácie so získanými výrazmi. Na tento účel sa pravá strana Mendelejevovej-Clapeyronovej rovnice vynásobí a vydelí číslom Avogadro. Teraz sa pozorne pozrieme na súčin množstva látky číslom Avogadro. Toto nie je nič iné ako celkový počet molekúl v plyne. Zároveň sa však pomer univerzálnej plynovej konštanty k číslu Avogadro bude rovnať Boltzmannovej konštante. Preto môžu byť vzorce pre tlak napísané takto: p=NkT/V alebo p=nkT. Symbol n je tu koncentrácia častíc.
Procesy ideálneho plynu
V molekulovej fyzike existuje niečo ako izoprocesy. Ide o termodynamické procesy, ktoré prebiehajú v systéme pri jednom z konštantných parametrov. V tomto prípade musí hmotnosť látky zostať konštantná. Pozrime sa na ne konkrétnejšie. Takže zákony ideálneho plynu.
Tlak zostáva konštantný
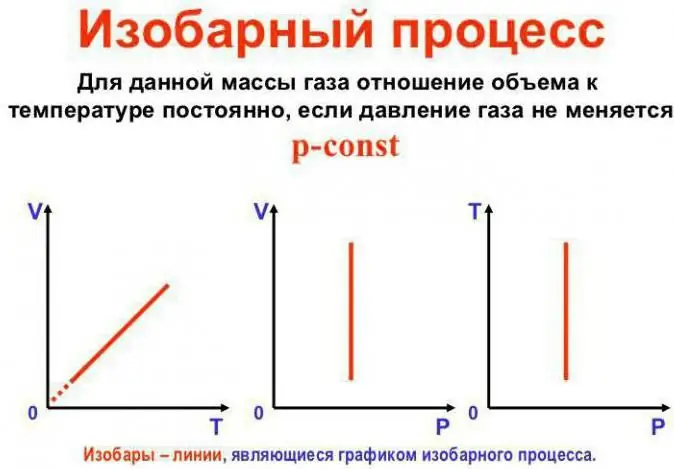
Toto je Gay-Lussacov zákon. Vyzerá to takto: V/T=konšt. Dá sa prepísať aj iným spôsobom: V=Vo (1 + at). Tu sa a rovná 1/273,15 K^-1 a nazýva sa "koeficient objemovej expanzie". Môžeme nahradiť teplotu v stupňoch Celzia ajKelvinovej stupnici. V druhom prípade dostaneme vzorec V=Voat.
Hlasitosť zostáva konštantná

Toto je druhý Gay-Lussacov zákon, bežnejšie označovaný ako Charlesov zákon. Vyzerá to takto: p/T=konšt. Existuje aj iná formulácia: p=po (1 + at). Transformácie sa môžu uskutočniť v súlade s predchádzajúcim príkladom. Ako vidíte, zákony ideálneho plynu sú si niekedy dosť podobné.
Teplota zostáva konštantná

Ak teplota ideálneho plynu zostáva konštantná, môžeme získať Boyleov-Mariottov zákon. Dá sa to napísať takto: pV=const.
Súvisiaci koncept 2: Čiastočný tlak
Povedzme, že máme nádobu s plynmi. Bude to zmes. Systém je v stave tepelnej rovnováhy a samotné plyny navzájom nereagujú. N tu bude označovať celkový počet molekúl. N1, N2 a tak ďalej, počet molekúl v každej zo zložiek zmesi. Zoberme si tlakový vzorec p=nkT=NkT/V. Dá sa otvoriť pre konkrétny prípad. Pre dvojzložkovú zmes bude mať vzorec tvar: p=(N1 + N2) kT/V. Potom sa však ukáže, že celkový tlak bude sčítaný z parciálnych tlakov každej zmesi. Takže to bude vyzerať ako p1 + p2 atď. Toto budú parciálne tlaky.
Na čo slúži?
Vzorec, ktorý sme získali, naznačuje, že tlak v systéme pochádza z každej skupiny molekúl. Mimochodom, nezávisí odiní. D alton to využil pri formulovaní zákona, ktorý bol neskôr po ňom pomenovaný: v zmesi, kde plyny navzájom chemicky nereagujú, bude celkový tlak rovný súčtu parciálnych tlakov.






