Štúdium vlastností ideálneho plynu je dôležitou témou fyziky. Úvod do charakteristík plynových sústav začína úvahou o Boyle-Mariotteovej rovnici, keďže ide o prvý experimentálne objavený zákon ideálneho plynu. Pozrime sa na to podrobnejšie v článku.
Čo znamená ideálny plyn?
Predtým, ako hovoríme o Boyle-Mariotteho zákone a rovnici, ktorá ho popisuje, definujme ideálny plyn. Bežne sa chápe ako tekutá látka, v ktorej častice, ktoré ju tvoria, navzájom neinteragujú a ich veľkosti sú zanedbateľne malé v porovnaní s priemernými vzdialenosťami medzi časticami.
V skutočnosti je každý plyn skutočný, to znamená, že jeho jednotlivé atómy a molekuly majú určitú veľkosť a neinteragujú medzi sebou pomocou van der Waalsových síl. Avšak pri vysokých absolútnych teplotách (viac ako 300 K) a nízkych tlakoch (menej ako jedna atmosféra) je kinetická energia atómov a molekúl oveľa vyššia ako energia van der Waalsových interakcií, takže skutočný plyn pri indikovanompodmienky s vysokou presnosťou možno považovať za ideálne.
Boyle-Mariotte rovnica
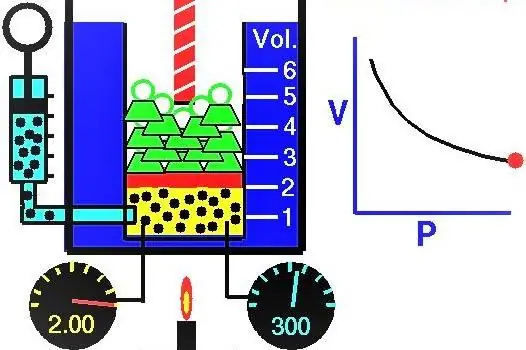
Vlastnosti plynov európski vedci aktívne skúmali počas XVII-XIX storočia. Úplne prvý zákon o plyne, ktorý bol experimentálne objavený, bol zákon popisujúci izotermické procesy expanzie a kompresie plynového systému. Zodpovedajúce experimenty vykonali Robert Boyle v roku 1662 a Edm Mariotte v roku 1676. Každý z týchto vedcov nezávisle ukázal, že počas izotermického procesu v uzavretom plynovom systéme sa tlak mení nepriamo úmerne objemu. Experimentálne získané matematické vyjadrenie procesu je napísané v nasledujúcom tvare:
PV=k
Kde P a V sú tlak v sústave a jej objem, k je nejaká konštanta, ktorej hodnota závisí od množstva plynnej látky a jej teploty. Ak vytvoríte závislosť funkcie P(V) na grafe, bude to hyperbola. Príklad týchto kriviek je uvedený nižšie.
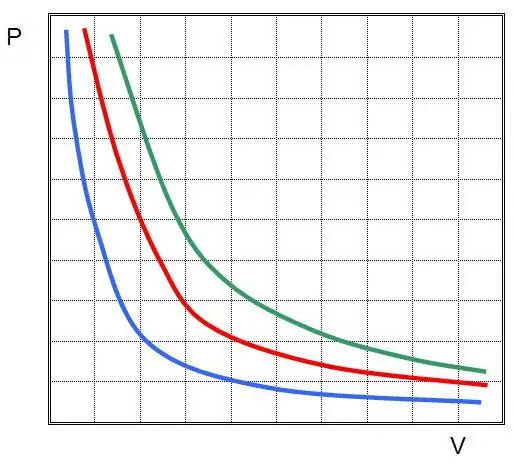
Písaná rovnosť sa nazýva Boyle-Mariotte rovnica (zákon). Tento zákon možno stručne sformulovať takto: expanzia ideálneho plynu pri konštantnej teplote vedie k proporcionálnemu zníženiu tlaku v ňom, naopak, izotermická kompresia plynového systému je sprevádzaná proporcionálnym zvýšením tlaku v ňom.
Rovnica ideálneho plynu
Boyleov-Mariottov zákon je špeciálnym prípadom všeobecnejšieho zákona, ktorý nesie mená Mendelejev aClapeyron. Emile Clapeyron, ktorý zhrnul experimentálne informácie o správaní plynov za rôznych vonkajších podmienok, získal v roku 1834 nasledujúcu rovnicu:
PV=nRT
Inými slovami, súčin objemu V plynovej sústavy a tlaku P v nej je priamo úmerný súčinu absolútnej teploty T a látkového množstva n. Koeficient tejto úmernosti sa označuje písmenom R a nazýva sa plynová univerzálna konštanta. V napísanej rovnici sa hodnota R objavila v dôsledku nahradenia množstva konštánt, ktoré vytvoril Dmitrij Ivanovič Mendelejev v roku 1874.
Z univerzálnej stavovej rovnice je ľahké vidieť, že stálosť teploty a látkového množstva zaručuje nemennosť pravej strany rovnice, čo znamená, že aj ľavá strana rovnice zostane konštantná. V tomto prípade dostaneme Boyleovu-Mariottovu rovnicu.

Iné zákony o plyne
Clapeyron-Mendelejevova rovnica napísaná v odseku vyššie obsahuje tri termodynamické parametre: P, V a T. Ak je každý z nich pevný a ostatné dva sa môžu meniť, dostaneme Boyleovu-Mariottovu rovnicu, Charlesove a Gay-Lussacove rovnice. Charlesov zákon hovorí o priamej úmernosti medzi objemom a teplotou pre izobarický proces a Gay-Lussacov zákon hovorí, že v prípade izochorického prechodu sa tlak plynu zvyšuje alebo znižuje priamo úmerne absolútnej teplote. Zodpovedajúce rovnice vyzerajú takto:
V/T=const, keď P=const;
P/T=const, keď V=const.
TakžeBoyle-Mariottov zákon je teda jedným z troch hlavných zákonov o plyne. Od ostatných sa však líši z hľadiska grafickej závislosti: funkcie V(T) a P(T) sú priame čiary, funkcia P(V) je hyperbola.
Príklad úlohy na aplikáciu zákona Boyle-Mariotte
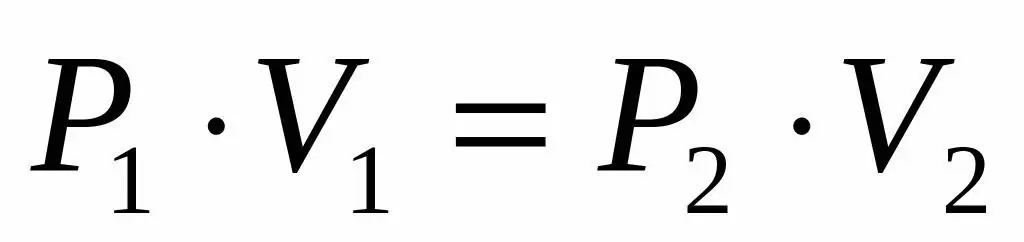
Objem plynu vo valci pod piestom v počiatočnej polohe bol 2 litre a jeho tlak bol 1 atmosféra. Aký bol tlak plynu po zdvihnutí piestu a zväčšení objemu plynovej sústavy o 0,5 litra. Proces sa považuje za izotermický.
Keďže máme daný tlak a objem ideálneho plynu a tiež vieme, že teplota zostáva nezmenená počas jeho expanzie, môžeme použiť Boyleovu-Mariottovu rovnicu v nasledujúcom tvare:
P1V1=P2V 2
Táto rovnosť hovorí, že súčin objemu a tlaku je konštantný pre každý stav plynu pri danej teplote. Vyjadrením hodnoty P2 z rovnosti dostaneme výsledný vzorec:
P2=P1V1/V 2
Pri výpočtoch tlaku môžete v tomto prípade použiť jednotky mimo systému, pretože litre sa zmenšia a dostaneme tlak P2 v atmosférách. Nahradením údajov z podmienky dospejeme k odpovedi na otázku problému: P2=0,8 atmosféry.






